Nedavno je kineska državna agencija za hranu i lijekove (SFDA) službeno prihvatila marketinšku primjenu tafolecimaba (PCSK-9 monoklonsko protutijelo koje proizvodi INNOVENT BIOLOGICS,INC), INC za liječenje primarne hiperkolesterolemije (uključujući heterozigotnu obiteljsku hiperkolesterolemiju i neobiteljsku hiperkolesterolemija) i mješovita dislipidemija.Ovo je prvi PCSK-9 inhibitor vlastite proizvodnje koji se prijavio za prodaju u Kini.
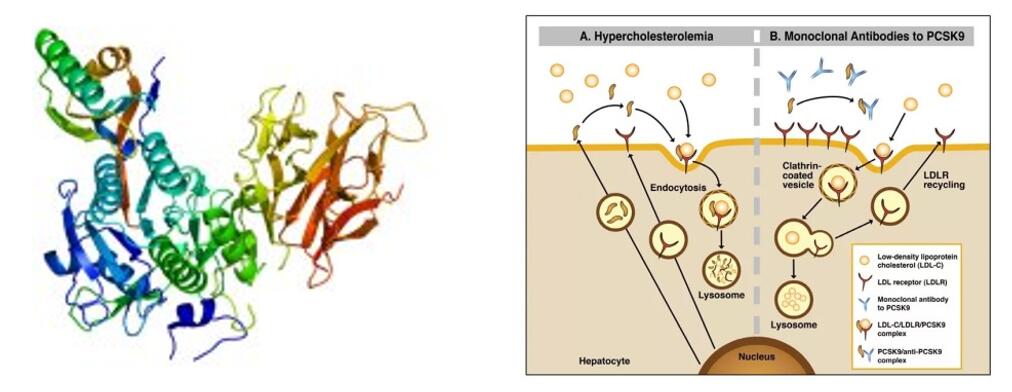
Tafolecimab je inovativni biološki lijek koji je neovisno razvio INNOVENT BIOLOGICS, INC. IgG2 ljudska monoklonska protutijela specifično vežu PCSK-9 za povećanje razine LDLR smanjenjem endocitoze posredovane PCSK-9, čime se povećava eliminacija LDL-C i snižavaju razine LDL-C.
Posljednjih godina, prevalencija dislipidemije značajno je porasla u Kini.Prevalencija dislipidemije i hiperkolesterolemije u odraslih je čak 40,4% odnosno 26,3%.Prema izvješću o kardiovaskularnom zdravlju i bolestima u Kini za 2020., stopa liječenja i kontrole dislipidemije kod odraslih još uvijek je na niskoj razini, a stopa usklađenosti LDL-C pacijenata s dislipidemijom još je manje zadovoljavajuća.
Prethodno su statini bili glavni tretman za hiperkolesterolemiju u Kini, ali mnogi pacijenti još uvijek nisu uspjeli postići cilj liječenja smanjenja LDL-C nakon liječenja.Marketing PCSK-9 donio je bolju učinkovitost pacijentima.
Podnošenje tafolecimaba od INNOVENT BIOLOGICS, INC temelji se na rezultatima triju kliničkih ispitivanja registriranih u demokratskoj fazi, ima dobar ukupni sigurnosni profil, sličan sigurnosnim karakteristikama proizvoda na tržištu, i postigao je duge intervale (svakih 6 tjedana) uprave.Rezultati studije CREDIT-2 prihvaćeni su na godišnjem sastanku Američkog kardiološkog fakulteta (ACC) 2022. kao sažetak i objavljeni na internetu.
Ako se zahtjev odobri, to će prekinuti mrtvu točku uvođenja PCSK-9, Kina će postati četvrta zemlja koja ima PCSK-9 nakon Sjedinjenih Država (Amgen), Francuske (Sanofi) i Švicarske (Novartis).
Vrijeme objave: 4. srpnja 2022